Patrones de seguimiento y manejo clínico multidisciplinario en pacientes con Mucopolisacaridosis tipo IVA en Colombia
Contenido principal del artículo
Resumen
Antecedentes: La información sobre el seguimiento y manejo de pacientes con mucopolisacaridosis IVA (MPS-IVA) con terapia de reemplazo enzimático (ERT) en Colombia es limitada.
Objetivos: Nuestro propósito es evaluar datos del mundo real de pacientes con MPS-IVA sometidos a ERT en Colombia para comprender sus perfiles, patrones de seguimiento y dinámicas del tratamiento.
Métodos: Se reclutó una muestra conveniente de genetistas y neurólogos pediátricos desde noviembre 2020 a enero 2021. Para cada paciente bajo su cuidado, los médicos respondieron un reporte basado en preguntas.
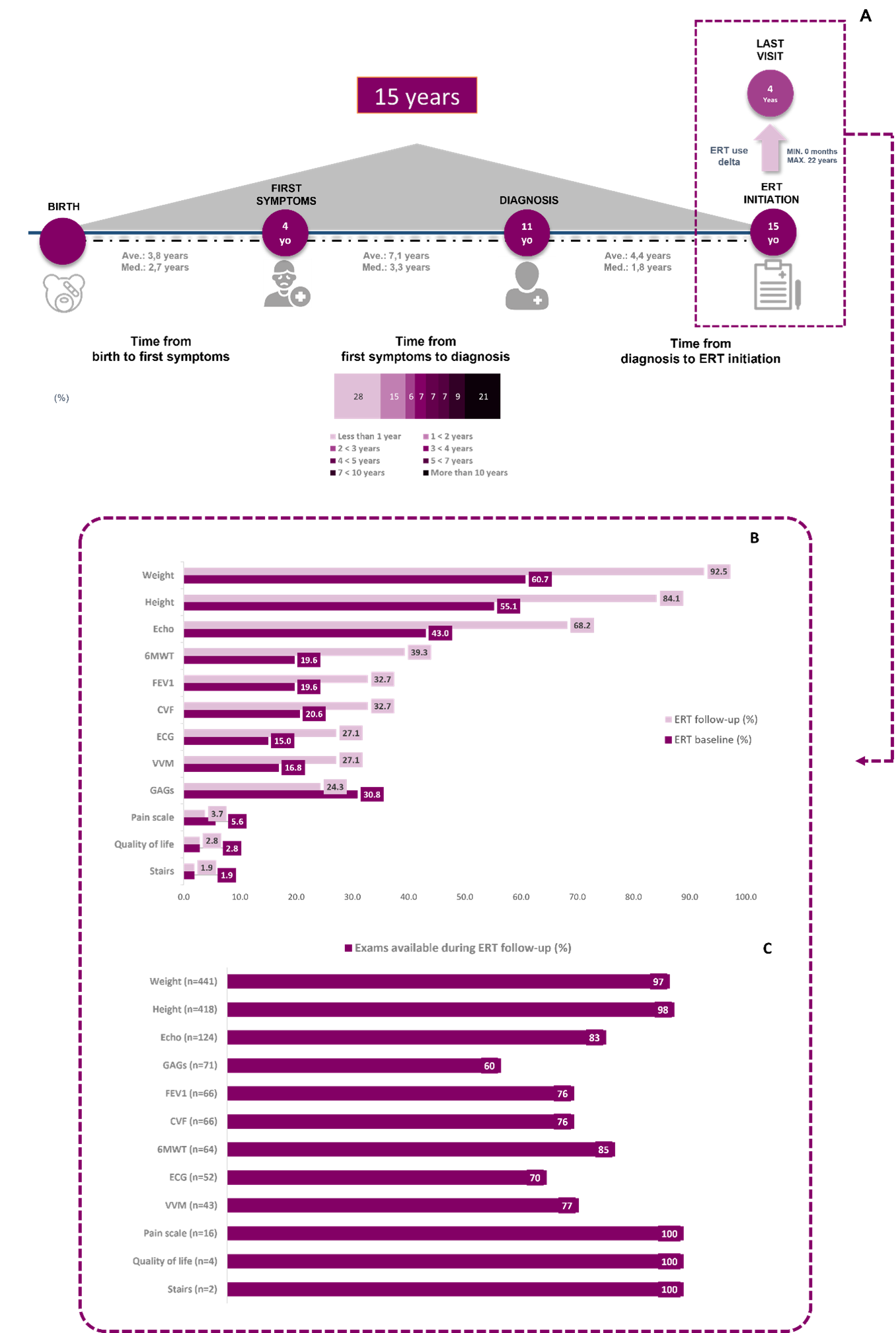
Resultados: Un total de 24 médicos (genetistas [92 %] y neuropediatras [8 %]) proporcionaron datos sobre 107 pacientes, diagnosticados mediante pruebas moleculares (36 %) y/o ensayos enzimáticos (97 %). Su edad promedio fue 19.5 años y 51% eran hombres. El tiempo promedio desde el primer síntoma al diagnóstico, del primer síntoma, del diagnóstico y de la primer ERT fue de 7.1, 4, 11 y 15 años, respectivamente. Los controles de seguimiento aumentaron post inicio de ERT; las evaluaciones más frecuentes fueron peso, altura y ecocardiografía; la calidad de vida, la prueba-de-caminata-de-6-minutos y la prueba de escaleras de 3 minutos fueron menos frecuentes. Se observaron interrupciones de ERT >2 meses en el 63 % de los pacientes.
Conclusiones: El monitoreo de pacientes con MPS-IVA que reciben ERT sigue siendo subóptimo en Colombia. Es necesario establecer pautas nacionales de manejo e implementar centros de referencia centralizados, donde los pacientes puedan recibir atención integral para garantizar sistemas, servicios y apoyo adecuados como prioridad, con un potencial efecto positivo en el curso de la enfermedad.
Descargas
Detalles del artículo

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-SinDerivadas 4.0.
Licencia Creative Commons
Atribución-NoComercial-CompartirIgual 4.0 Internacional (CC BY-NC-SA 4.0)
Usted es libre de:
Compartir - copiar y redistribuir el material en cualquier medio o formato.
Adaptar - remezclar, transformar y construir a partir del material
La licencia no puede revocar estas libertades en tanto se sigan los términos de la licencia.
- Atribución — Usted debe dar crédito de manera adecuada, brindar un enlace a la licencia, e indicar si se han efectuado cambios. Puede hacerlo en cualquier forma razonable, pero no de forma tal que sugiera que usted o su uso tienen el apoyo del licenciante.
- NoComercial — Usted no puede hacer uso del material con propósitos comerciales.
- CompartirIgual— Si remezcla, transforma o crea a partir del material, debe distribuir su contribución bajo la misma licencia del original.
- No hay restricciones adicionales — No puede aplicar términos legales ni medidas tecnológicas que restrinjan legalmente a otras a hacer cualquier uso permitido por la licencia.
Referencias
Morris CP, Guo XH, Apostolou S, Hopwood JJ, Scott HS. Morquio A syndrome: cloning, sequence, and structure of the human N-acetylgalactosamine 6-sulfatase (GALNS) gene. Genomics. 1994;22(3):652-4.DOI: 10.1006/geno.1994.1443. DOI: https://doi.org/10.1006/geno.1994.1443
Tomatsu S, Nishioka T, Montaño AM, Gutierrez MA, Pena OS, Orii KO, et al. Mucopolysaccharidosis IVA: identification of mutations and methylation study in GALNS gene. J Med Genet. 2004;41(7):e98.DOI: 10.1136/jmg.2003.018010. DOI: https://doi.org/10.1136/jmg.2003.018010
Zhou J, Lin J, Leung WT, Wang L. A basic understanding of mucopolysaccharidosis: Incidence, clinical features, diagnosis, and management. Intractable Rare Dis Res. 2020;9(1):1-9.DOI: 10.5582/irdr.2020.01011. DOI: https://doi.org/10.5582/irdr.2020.01011
Gómez A, Robles R, Suárez-Obando F. Estimación de las frecuencias de las mucopolisacaridosis y análisis de agrupamiento espacial en los departamentos de Cundinamarca y Boyacá. Biomédica: revista del Instituto Nacional de Salud. 2012;32.DOI: 10.7705/biomedica.v32i4.574. DOI: https://doi.org/10.7705/biomedica.v32i4.574
Pachajoa H, Acosta MA, Alméciga-Díaz CJ, Ariza Y, Diaz-Ordoñez L, Caicedo-Herrera G, et al. Molecular characterization of mucopolysaccharidosis type IVA patients in the Andean region of Colombia. Am J Med Genet C Semin Med Genet. 2021;187(3):388-95.DOI: 10.1002/ajmg.c.31936. DOI: https://doi.org/10.1002/ajmg.c.31936
Peracha H, Sawamoto K, Averill L, Kecskemethy H, Theroux M, Thacker M, et al. Molecular genetics and metabolism, special edition: Diagnosis, diagnosis and prognosis of Mucopolysaccharidosis IVA. Mol Genet Metab. 2018;125(1-2):18-37.DOI: 10.1016/j.ymgme.2018.05.004. DOI: https://doi.org/10.1016/j.ymgme.2018.05.004
Lavery C, Hendriksz C. Mortality in patients with morquio syndrome a. JIMD Rep. 2015;15:59-66.DOI: 10.1007/8904_2014_298. DOI: https://doi.org/10.1007/8904_2014_298
Hendriksz CJ, Harmatz P, Beck M, Jones S, Wood T, Lachman R, et al. Review of clinical presentation and diagnosis of mucopolysaccharidosis IVA. Mol Genet Metab. 2013;110(1-2):54-64.DOI: 10.1016/j.ymgme.2013.04.002. DOI: https://doi.org/10.1016/j.ymgme.2013.04.002
Hendriksz CJ, Berger KI, Giugliani R, Harmatz P, Kampmann C, Mackenzie WG, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet A. 2015;167a(1):11-25.DOI: 10.1002/ajmg.a.36833. DOI: https://doi.org/10.1002/ajmg.a.36833
Suarez-Guerrero JL, Gómez Higuera PJ, Arias Flórez JS, Contreras-García GA. [Mucopolysaccharidosis: clinical features, diagnosis and management]. Rev Chil Pediatr. 2016;87(4):295-304.DOI: 10.1016/j.rchipe.2015.10.004. DOI: https://doi.org/10.1016/j.rchipe.2015.10.004
Concolino D, Deodato F, Parini R. Enzyme replacement therapy: efficacy and limitations. Ital J Pediatr. 2018;44(Suppl 2):120.DOI: 10.1186/s13052-018-0562-1. DOI: https://doi.org/10.1186/s13052-018-0562-1
Mitchell JJ, Burton BK, Bober MB, Campeau PM, Cohen S, Dosenovic S, et al. Findings from the Morquio A Registry Study (MARS) after 6 years: Long-term outcomes of MPS IVA patients treated with elosulfase alfa. Mol Genet Metab. 2022;137(1-2):164-72.DOI: 10.1016/j.ymgme.2022.08.007. DOI: https://doi.org/10.1016/j.ymgme.2022.08.007
Long B, Tompkins T, Decker C, Jesaitis L, Khan S, Slasor P, et al. Long-term Immunogenicity of Elosulfase Alfa in the Treatment of Morquio A Syndrome: Results From MOR-005, a Phase III Extension Study. Clin Ther. 2017;39(1):118-29.e3.DOI: 10.1016/j.clinthera.2016.11.017. DOI: https://doi.org/10.1016/j.clinthera.2016.11.017
Schweighardt B, Tompkins T, Lau K, Jesaitis L, Qi Y, Musson DG, et al. Immunogenicity of Elosulfase Alfa, an Enzyme Replacement Therapy in Patients With Morquio A Syndrome: Results From MOR-004, a Phase III Trial. Clin Ther. 2015;37(5):1012-21.e6.DOI: 10.1016/j.clinthera.2014.11.005. DOI: https://doi.org/10.1016/j.clinthera.2014.11.005
Akyol MU, Alden TD, Amartino H, Ashworth J, Belani K, Berger KI, et al. Recommendations for the management of MPS IVA: systematic evidence- and consensus-based guidance. Orphanet J Rare Dis. 2019;14(1):137.DOI: 10.1186/s13023-019-1074-9. DOI: https://doi.org/10.1186/s13023-019-1074-9
Alvear-Sedan CC, Barboza-Ubarnes, M., y Grijalba-Romero, M. Ángel. Experiencia clínica y bioquímica de las mucopolisacaridosis en Cartagena de Indias, Colombia. Revista Ciencias Biomédicas. 2020;4(1):152–8.DOI: 10.32997/rcb-2013-2765.
Instituto Nacional de Salud. Informe de evento: Enfermedades Huérfanas - Raras. Primer semestre de 2022.
Céspedes Useche LP. Una mirada imageneológica, fisiopatológica y actualizada de las enfermedades huérfanas, desde la perspectiva real del departamento del Tolima. cientific and Educational Medical Journal. 2021;2(1):206-26.DOI: 2745-0252.
Alianza Iberoamericana de Enfermedades Huérfanas (ALIBER), Salazar Ceballos LV, Quiroga Carrillo M, Mesa Correa M, Suárez Obando F. Estudio ENSERio LATAM. Estudio sobre la situación de necesidades socio-sanitarias de las personas con enfermedades raras en latinoamérica. 2023. p. 5-51.
Guerrero R, Prada SI, Pérez AM, Duarte J, Aguirre AF. Universal health coverage assessment Colombia. Global Network for Health Equity. 2015.
Vallejo Alzate N, Hurtado PM. El Síndrome de Morquio en Colombia desde la molécula a la clínica. Pediatría. 2022;54(4):146-54.DOI: 10.14295/rp.v54i4.193. DOI: https://doi.org/10.14295/rp.v54i4.193
Solano VM, Mandujano CYC, Avila-Rejon CA, Espin VH, Montaño HPQ. Disease burden, management patterns and multidisciplinary clinical approaches for patients with MPS IVA and VI in selected Latin American Countries. Mol Genet Metab Rep. 2021;28:100769.DOI: 10.1016/j.ymgmr.2021.100769. DOI: https://doi.org/10.1016/j.ymgmr.2021.100769
Sawamoto K, Álvarez González JV, Piechnik M, Otero FJ, Couce ML, Suzuki Y, et al. Mucopolysaccharidosis IVA: Diagnosis, Treatment, and Management. Int J Mol Sci. 2020;21(4).DOI: 10.3390/ijms21041517. DOI: https://doi.org/10.3390/ijms21041517
Moreno Giraldo LJ, Escudero Rodriguez AM, Sanchez Gomez A, Satizabal Soto JM. Clinical and molecular characteristics of colombian patients with mucopolysaccharidosis IVA, and description of a new galns gene mutation. Mol Genet Metab Rep. 2018;16:53-6.DOI: 10.1016/j.ymgmr.2018.06.008. DOI: https://doi.org/10.1016/j.ymgmr.2018.06.008
Moreno Giraldo LJ, Satizábal JM, Sánchez Gómez A. Variantes del Complejo MPS en población Colombiana. Revista de la Asociación Colombiana de Ciencias Biológicas. 2020:124-42.DOI: 10.47499/revistaaccb.v1i32.213. DOI: https://doi.org/10.47499/revistaaccb.v1i32.213
Romo-Erazo L, Pérez-Restrepo R, Orozco-Hernández JP, Estrada-Álvarez JM, Porras-Hurtado GL. Hallazgos ecocardiográficos de pacientes pediátricos con mucopolisacaridosis tipo IV-A con mutación c.901G>T en el gen GALNS en un centro de salud de cuarto nivel de Colombia en el periodo de 2012-2019. Medicas UIS. 2022;35:19-25.DOI: 10.18273/revmed.v35n3-2022002. DOI: https://doi.org/10.18273/revmed.v35n3-2022002
Tapiero-Rodriguez SM, Acosta Guio JC, Porras-Hurtado GL, García N, Solano M, Pachajoa H, et al. Determination of genotypic and clinical characteristics of Colombian patients with mucopolysaccharidosis IVA. Appl Clin Genet. 2018;11:45-57.DOI: 10.2147/tacg.S141881. DOI: https://doi.org/10.2147/TACG.S141881
Harmatz PR, Lampe C, Parini R, Sharma R, Teles EL, Johnson J, et al. Enzyme replacement therapy outcomes across the disease spectrum: Findings from the mucopolysaccharidosis VI Clinical Surveillance Program. J Inherit Metab Dis. 2019;42(3):519-26.DOI: 10.1002/jimd.12079. DOI: https://doi.org/10.1002/jimd.12079
Politei J, Porras-Hurtado GL, Guelbert N, Fainboim A, Horovitz DDG, Satizábal JM. Enzyme replacement therapy interruption in mucopolysaccharidosis type IVA patients and its impact in different clinical outcomes. JIMD Rep. 2021;58(1):104-13.DOI: 10.1002/jmd2.12192. DOI: https://doi.org/10.1002/jmd2.12192
Harmatz P, Mengel KE, Giugliani R, Valayannopoulos V, Lin SP, Parini R, et al. The Morquio A Clinical Assessment Program: baseline results illustrating progressive, multisystemic clinical impairments in Morquio A subjects. Mol Genet Metab. 2013;109(1):54-61.DOI: 10.1016/j.ymgme.2013.01.021. DOI: https://doi.org/10.1016/j.ymgme.2013.01.021
Quijada-Fraile P, Arranz Canales E, Martín-Hernández E, Ballesta-Martínez MJ, Guillén-Navarro E, Pintos-Morell G, et al. Clinical features and health-related quality of life in adult patients with mucopolysaccharidosis IVA: the Spanish experience. Orphanet J Rare Dis. 2021;16(1):464.DOI: 10.1186/s13023-021-02074-y. DOI: https://doi.org/10.1186/s13023-021-02074-y
Hendriksz CJ, Lavery C, Coker M, Ucar SK, Jain M, Bell L, et al. Burden of disease in patients with Morquio A syndrome: results from an international patient-reported outcomes survey. Orphanet J Rare Dis. 2014;9:32.DOI: 10.1186/1750-1172-9-32. DOI: https://doi.org/10.1186/1750-1172-9-32
Ministerio de Salud y Protección Social. Guía para la habilitación de centros de referencia de diagnóstico, tratamiento y farmacias para la atención integral de las enfermedades huérfanas y la conformación de la red y subredes de centros de referencia para su atención. In: primaria Ddpdsya, editor. 2018.